|
|
МЕНЮ
|
Курсовая работа: Цитогенетическая и молекулярно-цитогенетическая характеристика микроделяционных синдромов Прадера-Вилли, Ангельмана и Ди ДжорджиГЛАВА 2. ХАРАКТЕРИСТИКА СИНДРОМОВ ПРАДЕРА-ВИЛЛИ И АНГЕЛЬМАНА 2.1 Цитогенетическая характеристика синдромов Прадера-Вилли и Ангельмана Наиболее убедительные данные получены при синдроме Прадера—Вилли (СПВ) и синдроме Ангельмана (СЭ), которые, имея существенно разные клинические проявления, в своей основе имеют сходные молекулярно-цитогенетические изменения (табл. 2 и 3). Таблица 2 Корреляция генотип-фенотип при синдроме Ангельмана
Таблица 3 Корреляция генотип—фенотип при синдроме Прадера-Вили
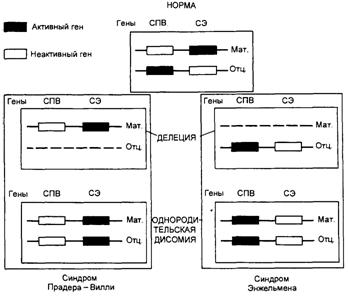
Наиболее частой причиной возникновения СПВ и СА является протяженная (до 4 млн. п.н.) деления критического района 15(q11—q13), которую находят у 70—75 % больных с этими синдромами. Делецию при СПВ обнаруживают на отцовской хромосоме 15, а при СЭ делеция той же области на ее материнском гомологе. Второй причиной возникновения СПВ и СЭ оказалась однородительская дисомия, т.е. наследование обоих гомологов хромосомы 15 от одного из родителей. С помощью ДНК-маркеров региона делеции путем блотт-гибридизации по Саузерну, а также анализа метилирования было продемонстрировано различное родительское происхождение хромосомы 15: в первом случае отцовское, во втором — материнское. Поскольку этот регион хромосомы 15 идентичен аналогичному региону хромосомы 2 мыши, для которого хорошо известен геномный импринтинг, исследования стали проводить в этом направлении. Оказалось, что регион СПВ активен на отцовской хромосоме (при наличии делеции на отцовской хромосоме или материнской ОРД отсутствуют отцовские гены) и не активен на материнской (рис. 3). Из рис. 1 видно, что при СПВ не экспрессируются отцовские гены, а при СЭ — материнские гены. Материнская ОРД наблюдается в 25 % случаев СПВ, а отцовская ОРД становится причиной возникновения СЭ в 3—5 % случаев [1]. В последние годы появились сообщения еще об одной причине развития этих синдромов у пациентов, у которых не было найдено ни типичных делеций, ни ОРД, но зато в семьях таких больных встречались повторные случаи синдрома. В ходе исследования в проксимальном участке хромосомы 15 были обнаружены противоположно импринтированные гены — кандидаты СПВ и СЭ, соответственно SNRPN и UBE3A, в которых выявили мутации.
Рис. 3 Механизмы возникновения синдромов Прадера—Вилли и Ангельмана через делецию участка хромосомы 15 или однородительскую дисомию по хромосоме 15. СПВ — синдром Прадера—Вилли; СА — синдром Ангельмана; мат. — материнская хромосома; отц. — отцовская хромосома Ген SNRPN кодирует полипептид N малого ядерного рибонуклеопротеина, активно экспрессируется исключительно на отцовской хромосоме 15 и репрессирован на материнском гомологе, т.е. мутации в этом гене вовлечены в патогенез СПВ. Критический регион для СЭ расположен дистальнее (локус D15S10), который экспрессируется только в материнских хромосомах. Предполагают, что мутации при СЭ есть в гене UBE3A кодирующем убиквитинлигазный белок ЗА. Экспрессия этого белка выявлена во всех тканях человека, причем в ряде структур мозга ген UВЕЗА активен лишь на материнской хромосоме. Дефицит материнской копии этого гена в клетках Пуркинье (грушевидных невроцитах мозжечка) и нейронах гиппокампа может, по-видимому, объяснить клиническую картину СЭ (умственная отсталость, атаксия, тремор и др.). Таким образом, в районе хромосомы 15(q11—q13) имеются близко расположенные, но противоположно импринтированные локусы, отвечающие за возникновение этих двух синдромов. Эта область хромосомы 15 чрезвычайно существенна для нормальной переустановки геномного импринтинга. Она названа центром импринтинга (IC). Мутации в данной области приводят к ошибкам импринтинга, т.е. теряется способность стирать отпечаток предшествующего поколения. Так, если в сперматогенезе отца не происходит замены «женского» импринта на «мужской» на его материнской хромосоме, то в следующем поколении возникнет состояние, аналогичное материнской ОРД, которое будет сопровождаться фенотипом СПВ. Нарушение установления «женского» эпигенотипа на отцовских хромосомах в овогенезе матери приведет к развитию СА у потомства. Повторный риск для трех групп семей при СПВ и СЭ будет существенно различаться. Так, при делециях он будет ниже 1 %, при ОРД риск также низкий, но в этом случае нужно учитывать возраст матери, который может увеличивать риск. При мутациях в центре импринтинга повторный риск будет существенно выше не только для родителей больного, но и ближайших родственников. Связь геномного импринтинга с другой наследственной патологией человека на уровне хромосом или отдельных генов также отчетливо прослеживается и в настоящее время широко изучается. Так, например, при хорее Гентингтона и спинно-мозжечковой атаксии I заболевание возникает раньше и протекает тяжелее, если унаследованные гены имеют отцовское происхождение. При нейрофиброматозе 1 и 2, миотонической дистрофии, наоборот, заболевание имеет более раннее начало и тяжелое течение при унаследовании мутантных генов от матери. Не вызывает сомнения причастность геномного импринтинга к этиологии опухолевого роста. Выключение импринтинга, а также потеря гетерозиготности или ОРД по хромосомам или их участкам, содержащим импринтированные локусы, могут приводить к функциональной нуллисомии генов-супрессоров опухолевого роста или к аберрантной экспрессии протоонкогенов, что может лежать в основе возникновения рака. Кроме того, вероятность ОРД повышается не только с возрастом матери, но и у носителей изохромосом, робертсоновских и реципрокных транслокаций. Следует иметь в виду, что ОРД (изодисомия) может привести к гомозиготизации определенных регионов хромосомы и быть причиной аутосомно-рецессивной патологии. Такие случаи описаны, например, при муковисцидозе. |
Copyright © 2012 г.
При использовании материалов - ссылка на сайт обязательна.